Pages
112
R.F. Weinland und Hans Schmid, Zeit anovg. Chem. 44, 37, 1905
SbCl6 4 1/2 H20 Metachlorantimusäure
Man lößt Antineonoxyd in etwa dur doppelten Menge konzentrierter Salzsäure und leitet Chlor bis zur völligen Sättigung in diese Lösung ein. Beim Einleiten färbt sich die Flüssigkeit zumächtet dunkler, dann bei weiterem Einleiten hell grünlich-gelb. Die Lösung wird auf dem Wasserbade etwas konzentriert, chloreowassartoff eingeleitet und zur Kristallisation über Schwefel säme in die Kälte gefellt (Temperatur mindestens 0). Es erleichtet die Kristallisation, wenn man die Lösung mit einem Kristall der Säure nimpft. Die Ausbeute ist sehr gut und die Säure ist nach dem Abpressen auf Ton und Truckneu über Schwefelsäure direkt rein.
Sie bildet Aggregate übereinander geschickteter, dichtur, flacher, gut begrenstiv Prismen, von der grünlichgelben Farbe des Chlors. Die Kristalle sind sehr hygroskopich und vermittern all mählich über Schwefelsäure
Die Säure ist im Wasser unter Abkühlung, fenner in Alkohol, Aceton und Eisessig sehr leicht klar löslich. Die Lösungen im Alkohol und Aceton reagieren neutral. Die wässerige Lösung der Säure scheidet beim stehen, nebueller beim Kochen, Antimonsäure ab. Die Lösung in 10% Salzsäure bleibt beim Stehen und beim Kochen klar. Lösungen im schwächerer Salzsäure Trüben sich je
113
nach dem Gebalt an Salzsäure mehr oder weniger rasch. Such Salpetersäure verlangsamt diese Zersetzung durch Wasser. Die Lösungen in Alcohol, Aceton und Eissessig hingegen bleiben sowohl beim Stehen als auch beim Kochen völlig klar Alkalien und Alkali karbonate scheiden aus der wässigen Lösung sofort Autimonsäure ab.
114
This page is not transcribed, please help transcribe this page
115
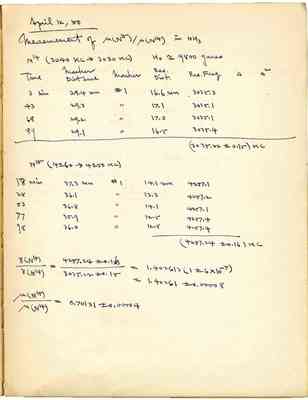
Atomic wt of nitrogen in 31.4% enriched N15 = 14.00751 × 0.686 + 15.00489 × 0.314 = 14.321
Gauss of HNO3 soln = 12.9 containing 10.57% nitric acid by wt.
Gauss of HNO3 = 0.1057 × 12.9 = 1.3635
Moles of HNO3 = 1.3635/63.329 = 0.02153
Molecular wt of NaNO3 = 85.32
Wt. of NaNo3 = 85.32 × 0.02153 = 18.34 1.834 grams
Soln of NaNO3 = 3.5 c.c.
Molar of soln =